審査手続き等ご案内
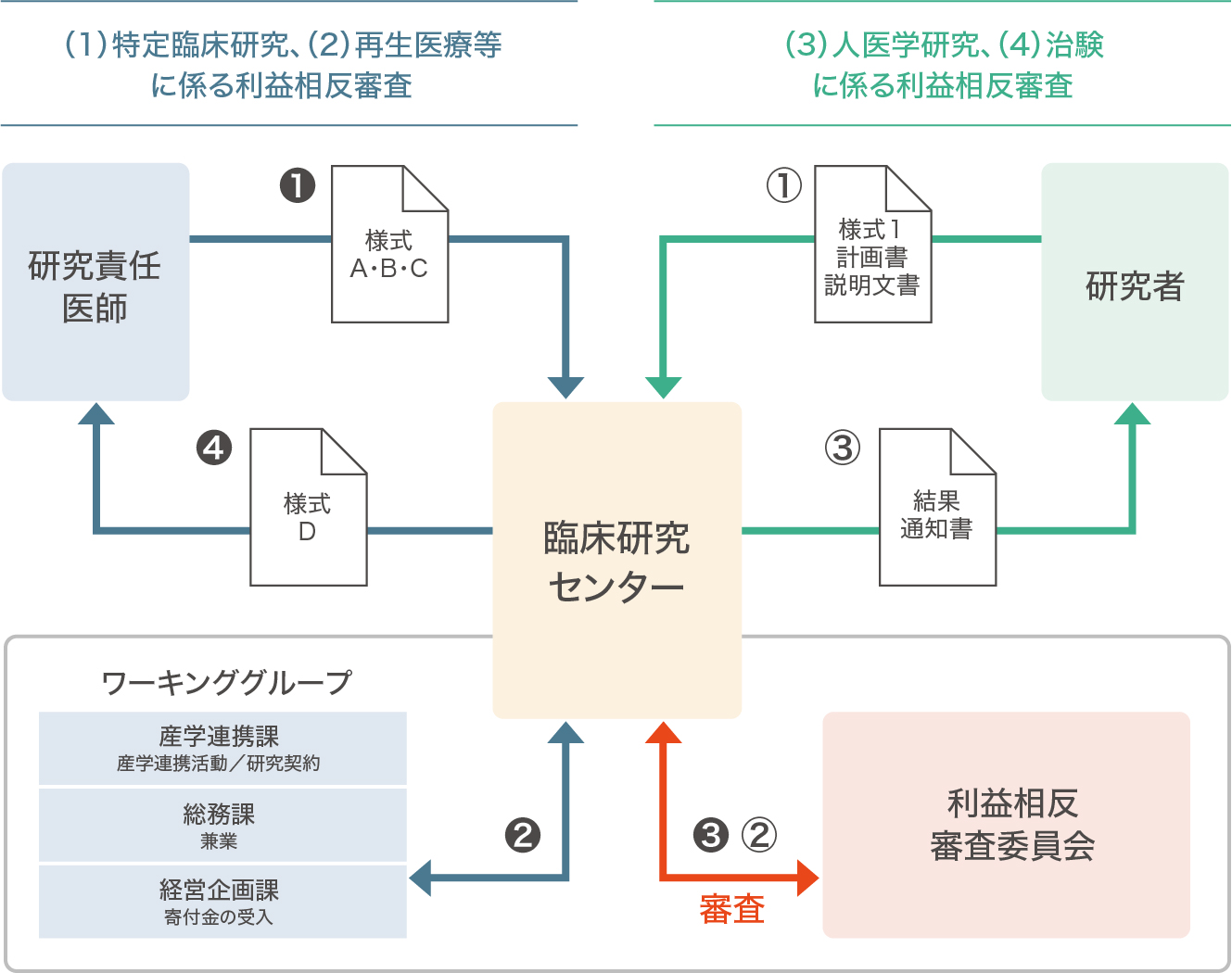
人を対象とする医学系研究等*にかかる利益相反申告は、該当する省令等によって様式や申告内容、審査スキームが異なります。以下に示す通常審査に加え、委員会で必要性が認められた場合に限り、迅速審査を行います。
*人を対象とする医学系研究等
(1) 臨床研究法(平成29年法律第16号)の対象となる研究
(2) 再生医療等の安全性確保等に関する法律(平成25年法律第85号)の対象となる再生医療等
(3) 人を対象とする医学系研究等に関する倫理指針(平成26年文部科学省・厚生労働省告示第3号)の対象となる研究
(4) 医薬品の臨床試験の実施の基準に関する省令(厚生省令第28号)の対象となる研究
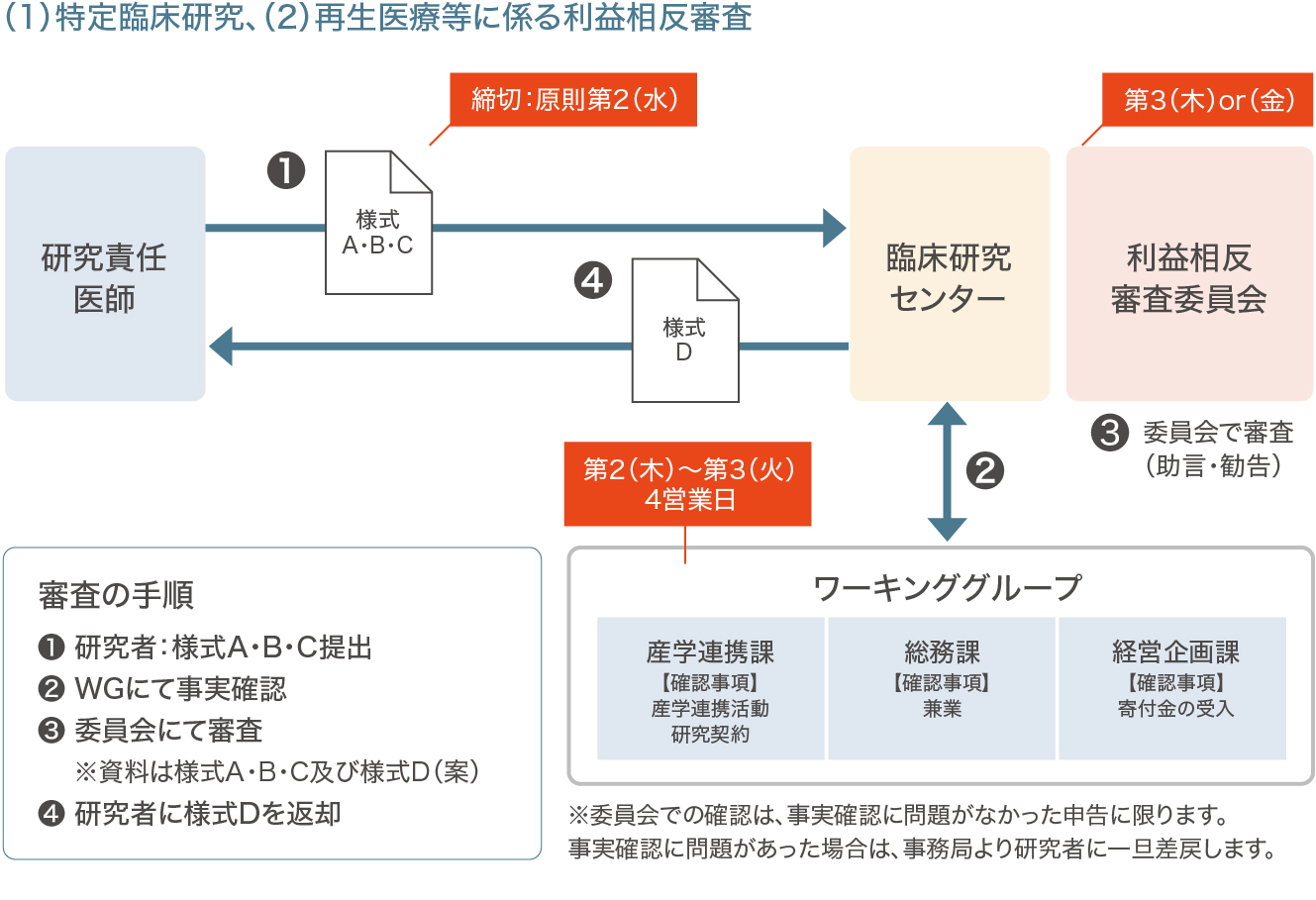
(1) 臨床研究法(平成29年法律第16号)の対象となる研究
臨床研究法に基づく「特定臨床研究」にかかる利益相反申告については、同法及び関係通知等をご確認下さい。様式もダウンロード可能です。
| 臨床研究法について(厚生労働省ホームページ) |
(2) 再生医療等の安全性確保等に関する法律(平成25年法律第85号)の対象となる再生医療等
再生医療等の安全性の確保等に関する法律に基づく「再生医療等」にかかる利益相反申告については、同法及び関係通知等をご確認下さい。様式もダウンロード可能です。
| 再生医療について(厚生労働省ホームページ) |
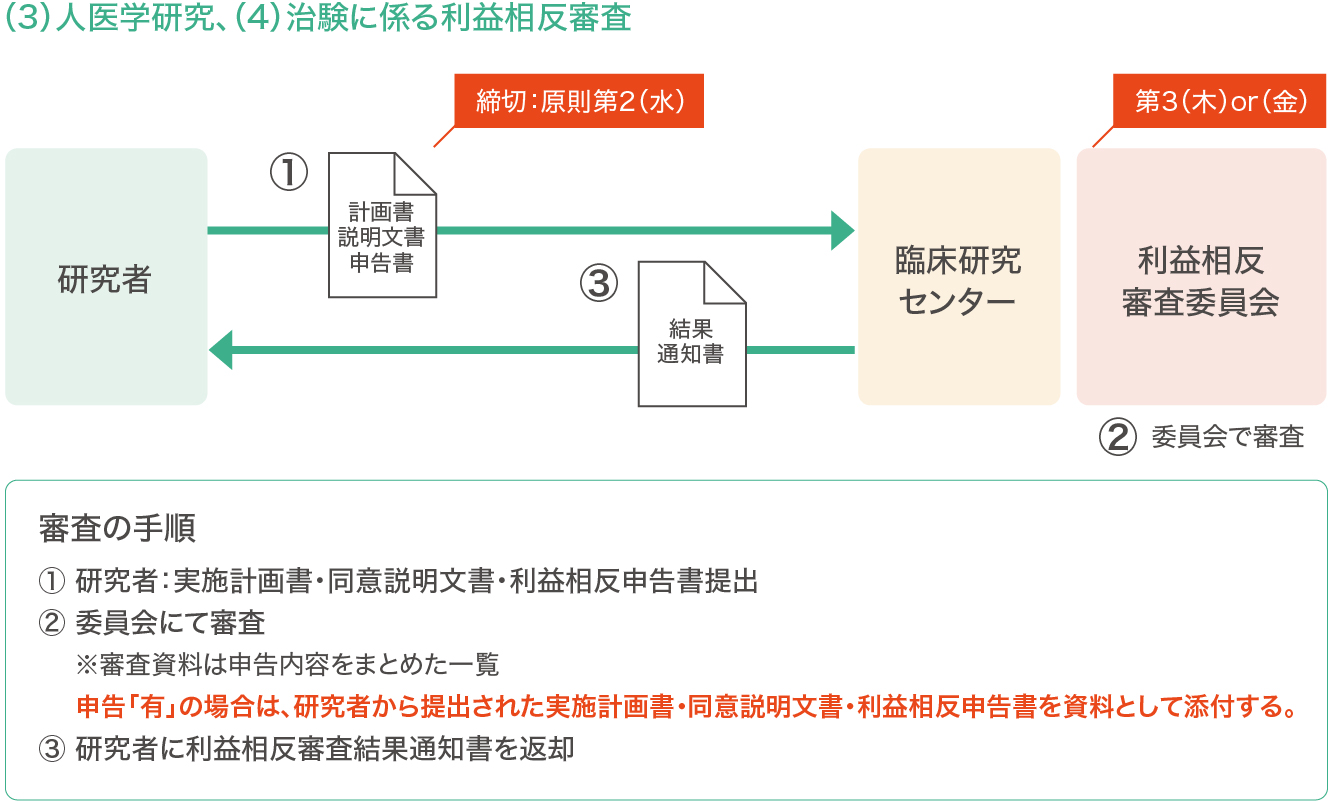
(3)人を対象とする医学系研究等に関する倫理指針(平成26年文部科学省・厚生労働省告示第3号)の対象となる研究
(4) 医薬品の臨床試験の実施の基準に関する省令(厚生省令第28号)の対象となる研究
山口大学の利益相反ポリシー等に従い、申告・審査が必要です。
| 様式1 利益相反申告書 |
研究の実施に際しては、各省令等に従ってください。
