倫理指針対応(申請手順)
人医学系研究等を実施する際は、適切な倫理審査申請手続きを行い、倫理審査委員会及び研究機関の長の「承認」を得る必要があります。
注意!
倫理審査申請手続きにはいくつかの段階があります。2.事前レビューから4.倫理審査までに早くとも2ヶ月程度の時間を要します。余裕をもって、ご準備ください。 研究開始までの流れは以下の通りです。
申請の流れ
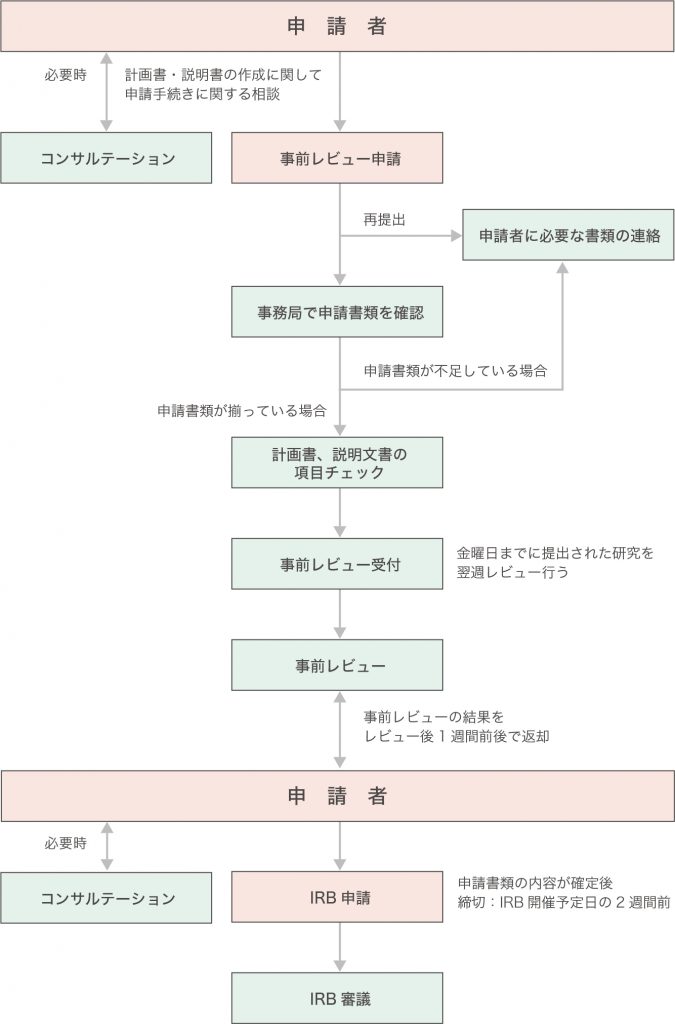
事前準備(コンサルテーション・書類作成等)
事前レビュー
捺印済み書類提出
倫理審査
研究開始
症例(事例)報告
山口大学医学部附属病院では、「症例報告に関する患者のプライバシー保護に関する指針」があります。 この指針に従い、症例報告を行うとともに、患者さんに症例報告を実施すること(実施が想定される場合も含む)の同意が取得できるような場合においては、 「山口大学医学部附属病院で診療を受けられる皆様へ」の説明文書を用いて、包括的な同意を取得することをお勧めいたします。
なお、本説明文書を用いて同意取得したことで、臨床研究等を実施する際の同意を取得したと見なすとはできません。 臨床研究等を開始する際には、研究ごとに患者さんに対し同意を取得することが原則です。 包括的な同意を取得していた場合、一部同意が免除される場合もありますが、研究の内容によってその対応は異なります。 その際には臨床研究センター(内線:2428)にご連絡ください。
| 症例報告に関する患者のプライバシー保護に関する指針 | |
| 山口大学医学部附属病院で診療を受けられる皆様へ(同意書) | |
| 症例報告申請書 |
